Phân tích mẫu hợp chất tạo bởi 2 nguyên tố sắt và oxi.Kết quả cho thấy thành phần phần trăn theo khối lượng của Fe trong hợp chất là 72,414%
a ) Viết CTHH và tính PTK của hợp chất
b ) Xác định hóa trị của sắt trong hợp chất .
Bài 3: Phân tích một mẫu hợp chất tạo bởi hai nguyên tố Fe và O. Kết quả cho thấy cứ 7 phần khối lượng Fe có tương ứng với 3 phần khối lượng O
a. Viết CTHH và tính PTK của hợp chất
b. Xác định hóa trị của Fe trong hợp chất.
CTHH : Fe2O3
hóa trị :
a . x = y.b
=> a .2 = 2.3
=> a = lll
: Phân tích một mẫu hợp chất tạo bởi 2 nguyên tố là Fe và O. Kết quả cho thấy cứ 7 phần khối lượng Fe có tương ứng với 3 phần khối lượng oxi.
a. Viết công thức hóa trị của Fe trong hợp chất
b. Xác định hóa trị của Fe trong hợp chất
Vậy x=2, y=3
Công thức hóa học của hợp chất là 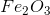
Phân tử khối bằng
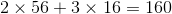
b) Hóa trị của Fe trong hợp chất là : III
Phân tích một mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần khối lượng sắt có tương ứng với 3 phần khối lượng oxi. Xác định hóa trị của sắt trong hợp chất.
Hợp chất Fe2O3. Gọi hóa trị của Fe là x
Theo quy tắc hóa trị ta có: x. 2 = 3.II ⇒ x = III
Phân tích một mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần khối lượng sắt có tương ứng với 3 phần khối lượng oxi. Viết công thức hóa học và tính phân tử khối của hợp chất.
Công thức chung của hợp chất F e x O y .
Theo đề bài ta có:
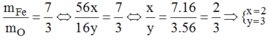
Vậy CTHH của hợp chất là F e 2 O 3 .
Phân tử khối là: 56.2 + 16.3 = 160 (đvC)
Phân tích mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi . Kết quả cho thấy cứ 7 phần khối lượng sắt có 3 phần khối lượng oxi.
a) Viết CTHH và tính PTK của hợp chất
b) Xác định hóa trị Sắt trg hợp chất
Ta có gọi CTHC là FexOy
=> \(\dfrac{56x}{16y}=\dfrac{7}{3}\)
=> \(\dfrac{x}{y}=\dfrac{7\times16}{3\times56}\)
=> \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHC là Fe2O3
a) Hợp chất tạo bởi nguyên tố Y ( hóa trị a) và nhóm NO3 có thành phần khối lượng là 34,043% Y. Xác định khối lượng mol của Y theo a?
b) R kết hợp với nguyên tố Oxi tao hợp chất X. Tính phần trăm khối lượng nguyên tố R trong X ?
Đ
ặ
t
:
Y
(
N
O
3
)
2
V
ì
:
%
m
Y
=
34
,
043
%
⇔
M
Y
M
Y
+
124
=
34
,
043
%
⇔
M
Y
=
64
(
g
m
o
l
)
⇒
Y
:
Đ
ồ
n
g
(
C
u
=
64
)
⇒
C
T
H
H
:
C
u
(
N
O
3
)
2
Thu gọn
1 hợp chất tạo bởi 2 nguyên tố sắt và oxi. Cho biết Tp% theo khối lượng của sắt trong hợp chất là 72,414%.
a) Xác định CTHH và PTK của hợp chất.
b) Xác định hóa trị của sắt trong hợp chất.
CÁC BẠN GIÚP MÌNH NHANH NHANH VỚI NHAAAAAA!
a/ CTHH của h/c: \(Fe_xO_y\left(x,y\in N;x,y>0\right)\)
Có: \(\frac{x}{y}=\frac{\%_{Fe}}{M_{Fe}}:\frac{\%_O}{M_O}=\frac{72,414}{56}:\frac{27,586}{16}\)\(=\frac{3}{4}\)
Vây CTHH:\(Fe_3O_4\)
PTK:\(M_{Fe_3O_4}=56.3+16.4=232\left(đvC\right)\)
b) Có:\(Fe_3O_4=FeO.Fe_2O_3\)
Vậy sắt có hóa trị: \(=II\left(trongFeO\right);III\left(trongFe_2O_3\right)\)
%O = 100- 72.414 =27.586%
Gọi: CTHH : FexOy
x : y = 72.414/56 : 27.586/16 = 3 : 4
Vậy: CTHH là : Fe3O4
MFe3O4 = 56*3 + 4*16 = 232 đvc
b)
Vì : Fe3O4 là hỗn hợp của 2 oxit : FeO và Fe2O3
=> Fe trong Fe3O4 sẽ mang 2 hóa trị là : II và III
. Mấy bn giúp mìh với:
Câu 1: Người ta xác định đc rằng ngtố Silic chiếm 87,5% về khối lượng trong hợp chất với ngtố Hiđro
a) Viết CTHH và tính PTK của hợp chất
b) Xác định hóa trị của Si trong hợp chất.
Câu 2: Phân tích mẫu hợp chất đc tạo bởi 2 ngtố Fe và O . Kết quả cho thấy 7 phần khối lượng Fe có tương ướng 3 phần O
a) Viết CTHH và tính PTK của hợp chất
b) Xác định hóa trị của Fe trong hợp chất.
câu 2
CTHH:Fe2O3 hay sắt 3 oxit
PTK:2x56+16x3=160
Fe hóa trị:2
a, Gọi công thức của hợp chất Si và H là SixHy(x,y nguyên dương)
%H=100%-87,5%=12,5%
Ta có tỉ lệ:x:y=%Si/M(Si) : %H/M(H)
=87,5/28:12,5/1
=3,125:12.5
=1:4
=>CT:SiH4
PTK(SiH4)=28+4=32
b,Gọi hóa trị của Si là a(a nguyên dương)
Aps dụng quy tắc hóa trị: a*1=I*4
=>a=IV
=>hóa trị cuiar Silic trong hợp chất là 4
Hợp chất (A) gồm nguyên tố Fe và nhóm sunfat (S04). Biết rằng trong hợp chất A nguyên tố Fe chiếm 28% theo khối lượng
a) Tìm công thức hóa học của hợp chất
b) Tính PTK của hợp chất A
c) Tính khối lượng theo gam của 5 phân tử hợp chất A, xem 1đvc = 0,166.10 mũ -23 gam
\(CT:Fe_2\left(SO_4\right)_x\)
\(\%Fe=\dfrac{56.2}{56\cdot2+96x}\cdot100\%=28\%\)
\(\Rightarrow x=3\)
\(CT:Fe_2\left(SO_4\right)_3\)
\(M_A=56\cdot2+96\cdot3=400\left(đvc\right)\)
Khối lượng của 5 phân tử Fe2(SO4)3 là :
\(5\cdot400\cdot0.166\cdot10^{-23}=332\cdot10^{-23}\left(g\right)\)
a)
Gọi CTHH là $Fe_2(SO_4)_n$
Ta có :
$\%Fe = \dfrac{56.2}{56.2 + 96n}.100\% = 28\%$
$\Rightarrow n = 3$
Vậy CTHH là $Fe_2(SO_4)_3$
b)
$PTK = 56.2 + 96.3 = 400(đvC)$
c)
$5M_A = 400.5 = 2000(đvC)$
$m_A = 0,166.10^{-23}.2000 = 3,32.10^{-21}(gam)$